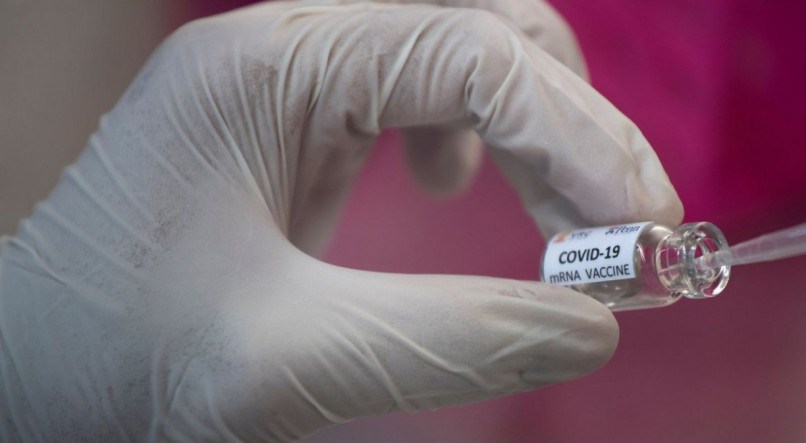
A Agência Nacional de Vigilância Sanitária (Anvisa) informou nesta terça-feira, 8, que recebeu comunicado do laboratório britânico AstraZeneca sobre a interrupção de estudos, que envolvem a Fiocruz, para desenvolver vacina contra a covid-19. Desenvolvida em parceria com a Universidade de Oxford, esta vacina é a aposta do governo Jair Bolsonaro (sem partido) para imunizar a população.
>> AstraZeneca suspende testes da vacina contra covid-19 após voluntário apresentar reações adversas
A agência disse que aguarda mais informações da AstraZeneca para se pronunciar oficialmente sobre a interrupção dos estudos. A decisão do laboratório britânico ocorre no dia em que o ministro interino da Saúde, Eduardo Pazuello, afirmou que em "janeiro a gente começa a vacinar todo mundo".
Os estudos envolvem diversos países e, segundo integrante do governo ouvido pelo Estadão, serão interrompidos também no Brasil. O governo federal abriu crédito de cerca de R$ 2 bilhões para a Fiocruz receber, processar, distribuir e passar a fabricar sozinha a vacina.
De acordo com fonte da Anvisa, o laboratório apenas enviou um comunicado à agência sobre a interrupção, sem detalhar que tipo de efeito colateral foi notado em participante do estudo, por exemplo, que levou a travar os trabalhos. Técnicos da Anvisa, agora, buscam mais informações da AstraZeneca.
"A decisão de interromper os estudos foi do laboratório, que comunicou os países participantes. A Anvisa já recebeu a mensagem e vai aguardar o envio de mais informações para se pronunciar oficialmente", disse a Anvisa em nota.



Comentários