Fundo Russo diz a governadores do Nordeste que precisa reavaliar envio da Sputnik V ao Brasil
O primeiro lote, contendo 1,1 milhão de doses para seis estados nordestinos, estava previsto para chegar ao Aeroporto do Recife no dia 28 de julho
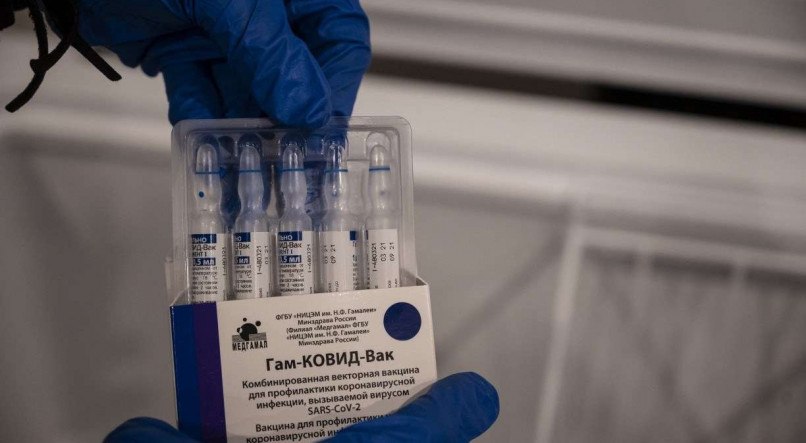
O Fundo Russo informou aos governadores do Nordeste nesta quarta-feira (21) que precisa de 48 horas para reavaliar o envio da vacina contra covid-19 Sputnik V. O motivo é uma declaração do ministro da Saúde, Marcelo Queiroga, que disse não haver necessidade de incorporar o imunizante fabricado na Rússia ao Plano Nacional de Imunizações (PNI). O primeiro lote, contendo 1,1 milhão de doses para seis estados, estava previsto para chegar ao Aeroporto do Recife no dia 28 de julho.
Em nota, o governador do Piauí e presidente do Consórcio Nordeste, Wellington Dias (PT), disse que o esforço dos governadores nordestinos para trazer a vacina tem sido uma corrida de obstáculos.
"Hoje, na agenda com os russos, depois que estava tudo já acertado para a próxima semana termos a entrega das vacinas, eles colocaram que precisavam avaliar essa situação do ministério em um prazo de 48 horas, e nós pedimos para que ficasse mantido o cronograma de entrega", explicou Dias.
O ministro da Saúde tinha dito no dia 14 de julho, em audiência na Comissão de Seguridade Social e Família da Câmara, que o número de doses contratadas pelo PNI será suficiente para vacinar toda a população brasileira acima de 18 anos com as duas doses contra a covid-19, até o fim deste ano. Como o volume estimado já obteve aval da Agência Nacional de Vigilância Sanitária (Anvisa), Queiroga disse que não há necessidade de incorporar doses adicionais como as da vacina Sputnik V e as da indiana Covaxin.
Na segunda-feira (19), os governadores do Nordeste solicitaram ao ministro da Saúde que ele se manifeste oficialmente sobre o tema. "Precisamos que o governo Federal defina se a Sputnik V será incorporada ao Plano Nacional de Imunizações e, então, podermos prosseguir com o contrato, que prevê a chegada das primeira doses no próximo dia 28 de julho", disse o secretário de Saúde de Pernambuco, André Longo, à coluna Saúde e Bem-Estar, deste JC. O secretário não informou o quantitativo que deve ser destinado a Pernambuco, e a assessoria de comunicação da Secretaria Estadual de Saúde (SES) disse que aguarda definições sobre o volume que será recebido.
A vacina Sputnik V foi adquirida pelos Estados integrantes do Consórcio Nordeste diretamente do Russian Direct Investment Fund (RDIF), sem intermediários, com cronograma de fornecimento que assegura entregas imediatas em quantitativos que permitem a ampliação da imunização da população brasileira. "Sem o retardo no processo de autorização e sem as arbitrárias condições restritivas impostas, que não consideram a situação calamitosa vivenciada pelos brasileiros e brasileiras, que choram mais de 500 mil mortes pela Covid-19, já teríamos vacinado com a Sputnik V mais de 37 milhões de brasileiros, de acordo com o cronograma originalmente pactuado neste mês de julho", destaca o ofício dos governadores do Nordeste enviado ao ministro Marcelo Queiroga.
Segundo dados do próprio Ministério da Saúde, trazidos no documento, aproximadamente 34 milhões de pessoas, em todo o Brasil, estão com o esquema vacinal completo contra a covid-19, o correspondente a tão somente 15,98% da população, "menos do que o quantitativo total da vacina Sputnik V adquirida, caso tivéssemos tido empenho das autoridades sanitárias e regulatórias para autorização de importação e uso".
Eficácia da Sputnik V
A vacina contra a covid-19 desenvolvida pela Rússia revelou uma eficácia de 91,6% contra as formas sintomáticas da doença, segundo resultados publicados em fevereiro na revista médica The Lancet e validados por especialistas independentes. Os resultados dizem respeito à última fase de ensaios clínicos da vacina, a fase três, que envolve cerca de 20 mil voluntários.
Os participantes no ensaio, realizado entre setembro e novembro de 2020, receberam todos duas doses da vacina ou um placebo com três semanas de intervalo. Em cada uma das doses, fizeram também um teste de PCR e, nos dias seguintes à administração da segunda dose, o teste foi realizado apenas em quem desenvolveu sintomas.
Um total de 16 voluntários dos 14,9 mil que receberam ambas as doses da vacina teve teste positivo (0,1%) em comparação com 62 de 4,9 mil voluntários que receberam o placebo (1,3%). Os autores apontam, no entanto, uma limitação: uma vez que os testes PCR só foram realizados quando os participantes declararam ter sintomas de covid-19, a análise da eficácia diz respeito apenas aos casos sintomáticos.
"São ainda necessárias mais pesquisas para determinar a eficácia da vacina em casos assintomáticos e na transmissão" da doença, explica a revista The Lancet em comunicado.
Termo
Os Estados do Nordeste, representados pelos seus governadores e secretários de Saúde, assinaram os Termos de Compromisso com a Anvisa para importação da vacina Sputnik V. Após as assinaturas, alguns condicionantes devem ser cumpridos previamente à chegada da vacina ao Brasil, como:
- Envio ao Instituto Nacional de Controle de Qualidade em Saúde (INCQS/Fiocruz) dos documentos e insumos necessários à realização das análises
- Envio à Anvisa de medida de mitigação do risco pelos fabricantes Generium e UfaVita, decorrente da ausência da validação da etapa de filtração esterilizante
- Envio à Anvisa do relatório final de validação do processo de fabricação do insumo farmacêutico ativo (IFA) ou declaração da autoridade russa de que verificou e aprovou tal documento
- Apresentação à Anvisa dos registros dos treinamentos dos operadores, indicando que os procedimentos de trabalho foram efetivamente corrigidos e não representam risco de contaminação ao produto
Mesmo após a chegada ao Brasil, segundo a Anvisa, a vacina só poderá ser utilizada após avaliação e liberação pelo INCQS, o que permitirá comprovar a ausência de vírus replicante na vacina e assegurar seus aspectos de qualidade e segurança.
"Destaca-se que a utilização da vacina no Brasil deverá ocorrer em condições controladas, com condução de estudo de efetividade executado conforme as Boas Práticas Clínicas", diz a Anvisa.

