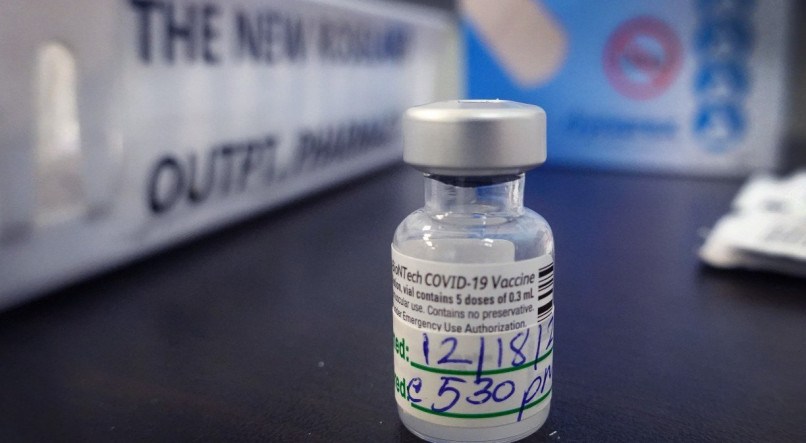
A Câmara dos Deputados aprovou, nesta sexta-feira (18), uma Medida Provisória (MP) que autoriza o governo federal a aderir ao consórcio Covax Facility, que é coordenado pela Organização Mundial da Saúde (OMS) e envolve governos, laboratórios e fabricantes com o objetivo de garantir o desenvolvimento de vacinas contra a covid-19 e o acesso igualitário a elas.
O texto-base foi aprovado em votação simbólica e agora vai ao Senado. Os deputados incluíram regras mais flexíveis para que a Agência Nacional de Vigilância Sanitária (Anvisa) conceda autorização temporária de uso emergencial para importação e distribuição de vacinas contra o vírus. Segundo o projeto, a Anvisa tem que responder ao pedido de uso emergencial em até cinco dias.
>> Tire as principais dúvidas sobre a vacina contra covid-19 no Brasil
>> STF decide que vacina contra a covid-19 pode ser obrigatória, mas não forçada
Segundo o governo, a adesão ao consórcio Covax Facility permitirá ao País negociar melhores termos com várias empresas e melhores condições para garantir o acesso às vacinas em cenário de intensa competição.
A adesão brasileira não implica a obrigatoriedade de compra das vacinas, que dependerá de análise técnica e financeira para cada caso. Devido à natureza do modelo, a aquisição dos produtos será feita sem licitação.
De acordo com o relator, a estimativa é que um total de 2 bilhões de doses de vacina sejam liberadas no âmbito desse instrumento até o final de 2021.
“No caso do Brasil, que conseguiu fechar acordos de forma bilateral com laboratórios, o Covax deve ser encarado como caminho alternativo, uma espécie de seguro, que pode ou não ser utilizado para ampliação de acesso e obtenção de número maior de doses”, afirmou.
Agências internacionais
Segundo o texto aprovado, a Agência Nacional de Vigilância Sanitária (Anvisa) concederá autorização temporária de uso emergencial para importação, distribuição e uso de qualquer vacina contra a covid-19.
Foi aprovado destaque da bancada do PDT para determinar que os estudos técnicos que embasarem decisões favoráveis ou contrárias à aquisição de vacinas serão publicados imediatamente após a conclusão, acompanhados da motivação das respectivas decisões.
A autorização da Anvisa terá de ser concedida em cinco dias a partir do pedido, desde que pelo menos uma de oito autoridades sanitárias internacionais relacionadas tenha aprovado o uso no próprio território.
O relator listou as dos Estados Unidos (FDA, na sigla em inglês); da União Europeia (EMA); do Japão (PMDA); da China (NMPA); do Canadá (HC); do Reino Unido (MHRA); e da Coreia do Sul (KDCA); mais o Ministério da Saúde da Rússia. A autoridade sanitária da Argentina (ANMAT) foi incluída no rol após a aprovação de destaque do PT.
As condições de registro e de autorização de uso deverão ser as mesmas do país de origem, e o fabricante deve se comprometer a concluir estudos clínicos em curso. A compra de vacinas poderá ser feita pela União ou por estados e municípios.
Aprovado, destaque do Cidadania inseriu no texto determinação para que, no caso das vacinas autorizadas, seja dispensada a assinatura de quaisquer termos de responsabilidade ou de consentimento por parte das pessoas, mesmo se a regra constar de outras normas.
Recursos
Por meio da MP 1004/20, o governo liberou recursos para integrar o consórcio. Do total de R$ 2,5 bilhões, deverá haver pagamento inicial de R$ 711,7 milhões ao Covax Facility, garantia financeira de R$ 91,8 milhões e pagamento adicional de R$ 1,71 milhão.
O relator especificou que a compra, pelo Ministério da Saúde, deverá ocorrer também com dotações orçamentárias do Programa Nacional de Imunização, no qual deverão ser incluídas todas as vacinas registradas perante a Anvisa.
Nessa aquisição, que poderá ser feita sem licitação, o governo federal deverá montar processo administrativo justificando o preço, indicando a escolha – se foi por meio do Covax Facility ou compra direta – e o atendimento de exigências sanitárias.
A compra, em igualdade de condições, dará preferência, pela ordem, à vacina produzida no Brasil; àquela produzida por empresa brasileira sediada no estrangeiro; ou a produzida por empresas que invistam em pesquisa e desenvolvimento de tecnologia no País.
Orientações
O texto aprovado prevê que a imunização a ser coordenada pelo Ministério da Saúde deverá seguir alguns parâmetros, ouvidos o Conselho Nacional de Secretários de Saúde (Conass) e o Conselho Nacional de Secretarias Municipais de Saúde (Conasems).
Entre os parâmetros destacam-se a compra centralizada; a distribuição universal, homogênea e equitativa; as parcerias com o setor privado para a divulgação da campanha de vacinação; os estudos de impacto das vacinas na mortalidade provocada pela doença e de seus eventos adversos; e a compra preferencial de produtores nacionais.
Já o plano nacional de imunização deverá garantir a compra e a distribuição dos insumos; a troca de informações; o monitoramento da campanha; a distribuição prioritária às unidades da Federação segundo critérios epidemiológicos; a inclusão no grupo de risco de profissionais de saúde, de segurança pública e de educação; e a imunização segura, eficaz e gratuita.
O texto aprovado determina ainda que, no caso de omissão ou de coordenação inadequada pelo Ministério da Saúde, os estados adotarão as medidas necessárias para imunizar sua população; e a União deverá arcar com as despesas.
Insumos
A compra de insumos também poderá ser feita sem licitação, incluindo-se ainda bens (como refrigeradores e outros), serviços de logística (distribuição no território), treinamento e serviços de informação.
O contrato deverá conter cláusulas sobre o regime de execução, preço, condições de pagamento, pagamento antecipado, garantias, penalidades, casos de rescisão, data e taxa de câmbio para conversão.
Transparência
Como medida de transparência, periodicamente, o Ministério da Saúde deverá publicar, na internet, uma série de dados relacionados às vacinas, assim como aqueles relacionados à compra, ao estoque e à distribuição de insumos (seringas, algodão etc).
O texto exige a divulgação, especificamente, da quantidade de vacinas compradas, o laboratório de origem, os valores pagos, os grupos elegíveis para a aplicação, a região onde ocorreu ou ocorrerá a imunização e o percentual de alcance da meta de vacinação.



Comentários