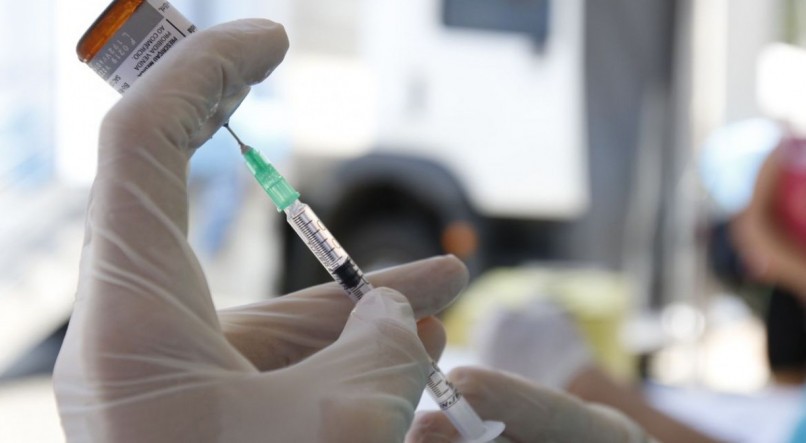
A vacina experimental contra a covid-19 desenvolvida pela farmacêutica americana Pfizer em parceria com a alemã BioNTech registrou 95% de eficácia nos resultados finais dos estudos e se mostrou segura. Na semana passada, as empresas haviam anunciado que a taxa de eficácia do potencial imunizante para o coronavírus havia sido de 90% nos resultados preliminares dos testes da fase 3.
A Pfizer também informou que planeja solicitar à Administração de Alimentos e Medicamentos dos Estados Unidos (FDA, na sigla em inglês) uma autorização de uso emergencial da vacina nos próximos dias, o que abriria caminho para que a distribuição começasse até o final de 2020, caso a agência reguladora aprove o pedido.
- Rússia diz que tem como fornecer ao Brasil 50 milhões de doses de vacina contra covid-19
- Vacina da Pfizer pode chegar ao Brasil no primeiro trimestre de 2021
- Brasil pode receber vacina da Pfizer até março; doses de Oxford devem ficar disponíveis em fevereiro
- Moderna anuncia outra vacina contra covid-19 com eficácia de mais de 90%
- Resultados de vacina da Moderna são 'incrivelmente impressionantes', diz Fauci à AFP
- Vacina chinesa Coronavac é segura e produz anticorpos contra covid-19 em 97% dos participantes, diz estudo de revista científica
De 170 voluntários adultos que desenvolveram covid-19 com pelo menos um sintoma, 162 receberam um placebo, enquanto oito receberam a vacina, disseram a Pfizer e a BioNTech. Ao todo, fizeram parte estudo quase 44 mil indivíduos.
Segundo as farmacêuticas, os pesquisadores não encontraram nenhum problema sério de segurança na vacina, que pareceu ser bem tolerada após uma revisão dos dados de 8 mil participantes. Um efeito colateral grave foi a fadiga, relatada por 3,8% dos indivíduos, de acordo com as empresas. Além disso, 2% dos indivíduos relataram dores de cabeça.
"Os resultados do estudo marcam um passo importante nesta jornada histórica de oito meses para apresentar uma vacina capaz de ajudar a acabar com esta pandemia devastadora", disse o CEO da Pfizer, Albert Bourla. "Continuamos avançando na velocidade da ciência para compilar todos os dados coletados até agora e compartilhar com os reguladores em todo o mundo", acrescentou.
De acordo com um porta-voz, a Pfizer está esperando para analisar completamente os dados e compilar a documentação necessária antes de pedir a autorização à FDA.



Comentários