Ministério da Saúde orienta suspensão da vacinação contra a covid-19 em adolescentes sem comorbidades
Texto argumenta falta de recomendações por órgãos internacionais e de pesquisas que evidenciem a segurança do imunizante em adolescentes sem comorbidades
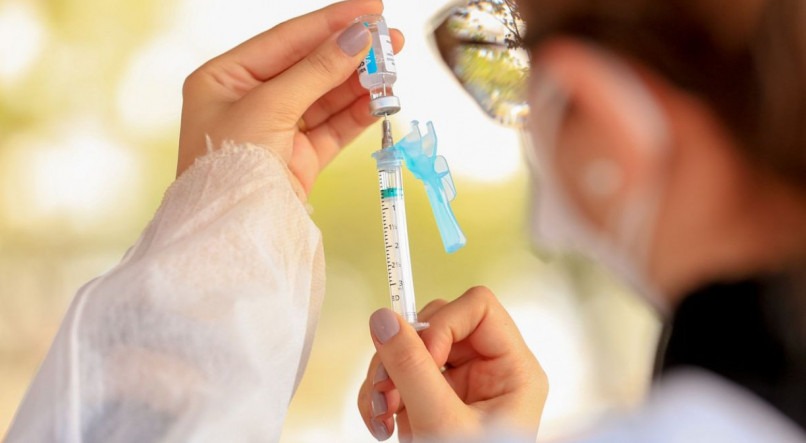
O Ministério da Saúde emitiu nessa quarta-feira (15) aos estados e municípios nota técnica que orienta a suspensão da vacinação contra a covid-19 em adolescentes (12 a 17 de anos) sem comorbidades. O Blog de Jamildo, do JC, divulgou que integrantes do Governo de Pernambuco tomaram conhecimento da nota nesta quinta (16) e a imunização desse grupo deve ser suspensa no Estado. A nota técnica argumenta que, apesar da autorização da Agência Nacional de Vigilância Sanitária (Anvisa) para uso da vacina Cominarty (Pfizer/Biontech) no grupo, há falta de recomendações por órgãos internacionais e de pesquisas que evidenciem a segurança do imunizante em adolescentes sem comorbidades.
"A Organização Mundial de Saúde não recomenda a imunização de criança e adolescente, com ou sem comorbidades; a maioria dos adolescentes sem comorbidades acometidos pela COVID-19 apresentam evolução benigna, apresentando-se assintomáticos ou oligossintomáticos; somente um imunizante foi avaliado em ECR", explicou.
"Os benefícios da vacinação em adolescentes sem comorbidades ainda não estão claramente definidos; apesar dos eventos adversos graves decorrentes da vacinação serem raros, sobretudo a ocorrência de miocardite (16 casos a cada 1.000.000 de pessoas que recebem duas doses da vacina); redução na média móvel de casos e óbitos (queda de 60% no número de casos e queda de mais de 58% no número de óbitos por covid-19 nos últimos 60 dias) com melhora do cenário epidemiológico", disse.
Por fim, a pasta reiterou que "revisará, sempre que necessário, suas recomendações, com base em dados de segurança e na evolução das evidências científicas".
A Saúde Estadual deve se manifestar nas próximas horas sobre o assunto, mas a tendência, segundo membros ouvidos pelo Blog de Jamildo sob reserva, é que haja orientação aos municípios pela suspensão da vacinação dos adolescentes sem comorbidades, que são doenças pré-existentes.
"O Governo de Pernambuco sempre seguiu as orientações do Ministério da Saúde. Defendo que a gente suspenda, apenas concluindo a vacinação agora naqueles que receberam a primeira dose", diz um membro da gestão estadual a par do andamento da imunização. Duas capitais, como Natal e Salvador, já anunciaram a suspensão nesta quinta-feira.
Anvisa se pronuncia
Após o Ministério da Saúde retirar nesta quinta-feira adolescentes de 12 a 17 anos sem comorbidades da lista de grupos cuja vacinação contra a covid-19 é recomendada, a Agência Nacional de Vigilância Sanitária (Anvisa) emitiu nota informando que mantém a orientação de imunizar a faixa etária com a Comirnaty, vacina desenvolvida pela Pfizer. Segundo o órgão, até o momento, não existem evidências que subsidiem ou demandem alterações nas condições aprovadas para a vacina.
- Covid-19: em Pernambuco, secretário critica recuo na vacinação de adolescentes sem comorbidades e diz que Estado continua a imunizá-los
- Ministro da Saúde, Queiroga diz que vacinação de adolescentes foi "intempestiva"
- Por que a vacinação em adolescentes foi suspensa? Veja quais países vacinam adolescentes e o que dizem estudos e a OMS
Ao justificar a decisão da Saúde, o ministro Marcelo Queiroga disse que foram identificados 1,5 mil eventos adversos em adolescentes imunizados. Todos eles foram de grau leve. Foi notificado um caso de morte de um jovem em São Paulo, mas o episódio ainda está sendo investigado para avaliar se a causa foi o imunizante.
Anvisa vai investigar morte
A Anvisa afirmou que vai investigar a morte de uma adolescente de 16 anos após aplicação da Pfizer, caso citado pelo ministro, mas, no momento, "não há uma relação causal definida entre este caso e a administração da vacina".
"A Anvisa já iniciou avaliação e a comunicação com outras autoridades públicas e adotará todas as ações necessárias para a rápida conclusão da investigação. Entretanto, com os dados disponíveis até o momento, não existem evidências que subsidiem ou demandem alterações nas condições aprovadas para a vacina", diz a agência.
